침습성 아스페르길루스증(invasive aspergillosis; IA)
장기 이식 환자, 장기간 면역억제제 치료를 받는 환자에서 침습성 아스페르길루스증의 위험이 높다.
IA를 진단하는데 증상과 징후는 비특이적이고 배양 검사는 시간이 오래 걸리며 민감도가 낮다는 문제점이 있다.
갈락토만난 항원 검사(galactomannan test)는 IA 진단 방법 중 비침습적이며 결과를 신속히 알 수 있어 진단에 유용하다.
갈락토만난이란?
아스페르길루스 균사 세포벽의 주성분
아스페르길루스가 혈관을 침범하여 자라는 동안 혈액 내로 방출
민감하게 1 ng/mL까지 항원을 검출할 수 있음

해석 시 유의
- 항진균제 사용: mold-active antifungal therapy 시 갈락토만난의 sensitivity 감소됨
- 일부 항생제 사용: 베타락탐/베타락탐 억제제인 tazocillin/sulbactam나 amoxicillin/clavulanic acid 제제를 사용하는 경우 위양성이 나올 수 있으므로 확진을 위해서는 반복해서 검사를 해야 함. tazocillin/sulbactam 투여 환자에서 위양성이 5일 동안 지속되었음. 하지만 이 항생제가 갈락토만난 분석에 영향을 끼치지 않음을 시사하는 연구 결과가 최근 나옴.
- 다른 유기체에 의한 교차 항원 반응: 아스페르길루스 뿐만 아니라 Fusarium species & others (Penicillium species, Histoplasma capsulatum)와 같은 유기체에서도 세포벽에 갈락토만난이 있어 교차 항원 반응이 나타날 수 있음.
- 특이 환자군: 위양성 결과는 조혈모세포이식 첫 100일 동안 발생할 가능성이 높으며 항암 화학 요법 또는 이식편성숙주질환(GVHD)으로 인한 위장관 점막염 환자(gastrointestinal tract mucositis)에서 발생할 가능성이 높음. 교차 반응성을 가지는 epitope(cross-reactive epitopes)를 가진 음식이나 유기체의 갈락토만난이 손상된 장점막을 가로질러 이동할 수 있다는 메커니즘으로 설명할 수 있음.
- 식품 오염: Aspergillus or closely related fungi, such as Penicillium spp에 의한 식품 오염으로 위양성이 발생할 수 있음. 아이스팝 포장지의 Penicillium 균에 의한 오염이나 sodium gluconate과 같은 아이스팝의 식품 첨가물이 원인으로 여겨짐.
- 병용 약제: 한 연구에서 intravenous immunoglobulin 투여받은 일부 환자들에게 위양성 결과를 보임
TPN 투여가 갈락토만난 시험 위양성을 야기한다?
Background: The detection of Aspergillus galactomannan antigenemia (GM-Ag) is a contributive method in the diagnosis of invasive aspergillosis (IA). Herein, we report 3 cases of false positive GM-Ag in paediatric patients (pts) receiving NP2 Enfants AP-HP® parenteral nutrition (Fresenius, France), and none of them had or developed IA.
Methods: In December 2006, the sera of these 3 pts (1 allogeneic transplant recipient and 2 neutropenic acute leukaemia pts) taken before, during, and after cessation of NP2 solution were tested for the presence of GM-Ag using the Platelia® Aspergillus kit. This solution, its 30 components and 8 other commercially available solutions for parenteral nutrition were tested for the presence of GM.

Results: GM became detectable within 1 day after IV administration of NP2 with indices up to 9.25, remained positive throughout treatment, and became negative (≤0.5) within 48 hours in 2/3 pts. The NP2 solution and a single one of its components, sodium gluconate (SG), tested positive with GM estimated at 55.4ng/ml. No Aspergillus DNA was detected by real-time PCR. Three NP2 and 6 SG batches from different origins yielded similar results. On the other hand, 6 different batches of calcium gluconate and 8 other commercially available SG-free parenteral nutrition solutions tested negative.
Conclusions: These results suggest a strong cross reactivity of Platelia® kit with SG-containing NP2, as recently described with Plasma-Lyte® (Baxter Distribution Centre Europe). We estimate that clinicians and biologists should become aware of this problem which might lead to inappropriate invasive investigations and/or treatments.
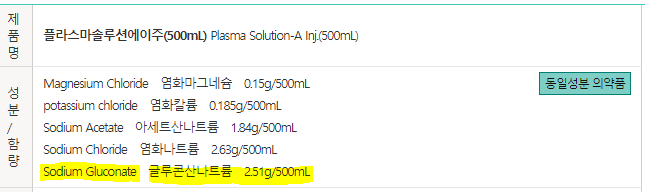



<In vitro 실험>
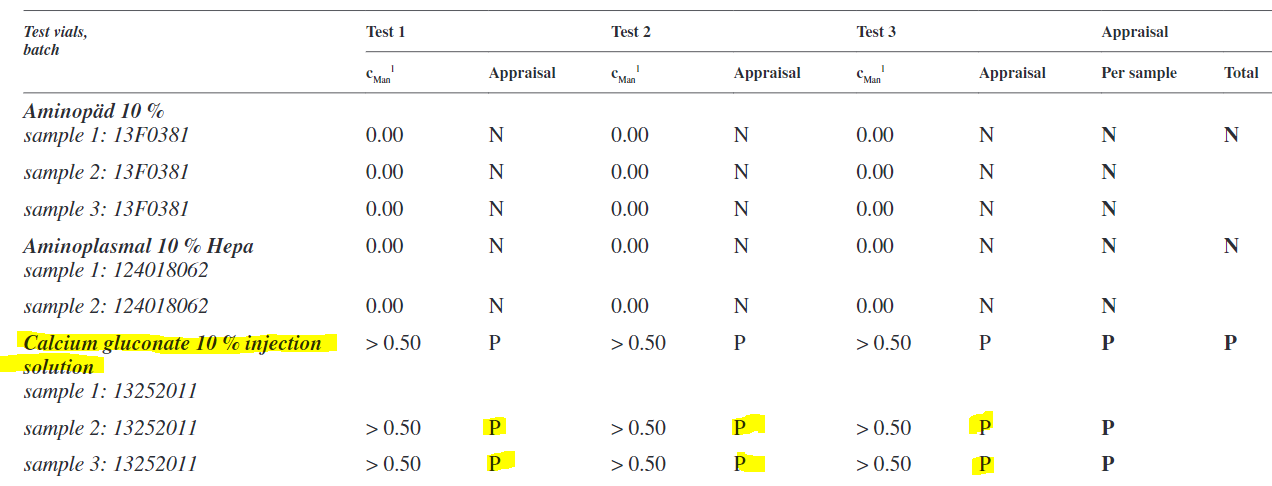

Results of Candida mannan EIA. The table presents the Candida antigen concentrations cMan1 of every tested sample and every test round in ng/ ml. Every result is considered positive (P), borderline (B) or negative (N) in the following column (“appraisal”). The two final columns sum-marize the appraisals per sample and per infusion solution in total. A positive result (P) is defined by a mannan concentration over 0.125 ng/ ml, a borderline result (B) by a mannan concentration between 0.0625 ng/ ml and 0.125 ng/ ml and a negative result by a mannan concentration below 0.0625 ng/ ml. Mannan concentrations over 0.5 ng/ ml are outside the measuring range.
They were considered positive with a concentration > 0.125 ng/ ml mannan (Tracitrans® infant, calcium gluconate solution) and borderline with a concentration between 0.0625 and 0.125 ng/ ml mannan (Tracitrans® plus, SMOFlipid®). None of the analysed infusions contained the Aspergillus galacto-mannan. In conclusion, further investigations on the topic are necessary to determine their in-vivo impact. A positive Platelia™ test result can simulate the presence of invasive fungal infections. As a consequence the patient may be treated with expensive, systemic antimycotics with a high risk of adverse events. Therefore a definite diagnosis is important.
<22.12.08> 추가
** Sodium gluconate가 galactomannan(GM) test에서 위양성을 일으키는 메커니즘
gluconate와 같은 저분자량 유기산(low-molecular-weight organic acid)은 Aspergillus niger and Aspergillus terreus의 발효 과정에 의해 생성된다. 의료 등급 gluconate 생성 당시 GM은 발효 용액으로 방출 혹은 여과, 분획 과정에서 운반될 수 있다. Plasma solution A와 같은 의약품은 멸균 상태이지만 분획 및 여과의 종류와 정도에 따라 gluconate 염 함유 용액에 GM은 여전히 남아있을 수 있으며 잠재적으로 GM test의 위양성을 야기할 수 있다.
Low-molecular-weight organic acids, such as gluconate, are produced by a fermentation process involving Aspergillus niger and Aspergillus terreus.
GM is released into the fermentation solution and is likely carried through the fractionation or filtration process for medical-grade gluconate.
Although Plasmalyte is sterile, GM may still persist in the gluconate-containing solution, depending on the type and extent of fractionation and filtration, potentially resulting in a false-positive serum and BAL fluid GM.
reference:
1) Vena, A., et al. "The misleading effect of serum galactomannan testing in high-risk haematology patients receiving prophylaxis with micafungin." Clinical Microbiology and Infection 23.12 (2017): 1000-e1.
2) http://snuhlab.org/checkup/check_view.aspx?no=1245
서울대학교병원 진단검사의학과
...
snuhlab.org
3) Ribaud, Patricia, et al. "Sodium gluconate containing parenteral nutrition solution as a cause of false positive aspergillus galactomannan assay in paediatric patients with hematological malignancies." (2007): 4958-4958.
4) Knoth, H., D. Maywald, and W. Walter. "In-vitro detection of mannan and galactomannan in components of total parenteral nutrition (TPN)." Die Pharmazie-An International Journal of Pharmaceutical Sciences 71.5 (2016): 238-242.
5) Spriet, Isabel, et al. "Plasmalyte: no longer a culprit in causing false-positive galactomannan test results." Journal of Clinical Microbiology 54.3 (2016): 795-797.
'🤹♂️ 카테고리별 약물 > 감염' 카테고리의 다른 글
| azithromycin 1250 mg vs 1200 mg : AIDS에서 기회감염증, MAC(Mycobacterium avium complex) prophylaxis (0) | 2023.02.18 |
|---|---|
| azithromycin의 재발견: MDR-Pseudomonas, outpatient, oral antibiotic (0) | 2023.02.17 |
| Vancomycin vs. Teicoplanin 약물 이상반응 비교 (0) | 2022.10.04 |
| 내성 결핵 치료 : Bedaquiline–Pretomanid–Linezolid Regimen (1) | 2022.09.11 |
| 복강 내 투여(Intraperitoneal; IP): 복막 투석 환자의 복막염 치료(PD, Peritonitis) (0) | 2022.06.20 |


댓글